¿Qué son las fuerzas intermoleculares? ¿Por qué las estudiamos?
➡️ Cuando pensamos en moléculas, sabemos que existen fuerzas de atracción que mantienen unidos sus átomos, éstos son las fuerzas intramoleculares (unión covalente); pero además existen otras fuerzas de atracción y son las que mantiene unidas a las moléculas entre sí, que son las
fuerzas intermoleculares. Porque no, no andan sueltas por ahí las moléculas, sino que están interactuando entre ellas.
Quiero que notes la diferencia entre las intramoleculares e intermoleculares, así que te dejo un esquemita a continuación. Tené en cuenta que las fuerzas intermoleculares son más débiles que las intramoleculares:
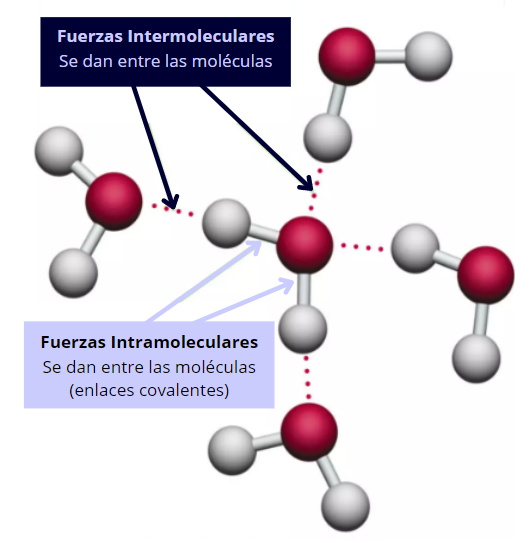
En esta parte de la materia nos vamos a enfoncar en las fuerzas intermoleculares.
Si vos tenés un vaso con agua, toooooodas esas moléculas de agua no están dispersas y solas en la nada misma, sino que están ahí, interactuando unas con otras, confiriéndoles propiedades a ese agua que, eventualmente te vas a tomar. ¿Estás tomando agüita? Mirá que es importante que te hidrates bien eh.. Bueno, sigamos..
¿Por qué nos interesa estudiar qué fuerzas existen entre las moléculas de una sustancia?
Bueno, porque ellas influyen directamente en propiedades como los puntos de fusión y ebullición, la volatilidad y la viscosidad de las sustancias.
Sustancias con fuerzas intermoleculares fuertes generalmente tienen puntos de ebullición y fusión más altos porque se requiere más energía para superar estas fuerzas y cambiar el estado de la sustancia.
Recordá que el punto de ebullición es la temperatura a la que ebulle una sustancia (pasa de estado líquido a gaseoso) y el punto de fusión es la temperatura a la que funde una sustancia (pasa de estado sólido a líquido).
También determinan la solubilidad de una sustancia en un solvente particular. La regla general "lo semejante disuelve a lo semejante" sugiere que sustancias con tipos similares de fuerzas intermoleculares tienden a ser solubles entre sí. Por ejemplo, las moléculas polares se disuelven bien en solventes polares, y las no polares se disuelven bien en solventes no polares.
👉 Hay muchas otras propiedades influidas por las fuerzas intermoleculares, pero excede a esta materia. Acá vamos a estudiar principalmente cómo éstas determinan los puntos de ebullición y la solubilidad.
¿Qué tipos de fuerzas intermoleculares hay? ¿Cómo puedo saber que tipos de fuerzas intermoleculares presenta una sustancia?
Eso lo vamos a ver en los videos que siguen 👉
¡Vamos!
🤖
¿Tenés dudas? Pregúntale a ExaBoti
Asistente de IA para resolver tus preguntas al instante🤖
¡Hola! Soy ExaBoti
Para chatear conmigo sobre este contenido necesitas desbloquear el curso
ExaComunidad
Conecta con otros estudiantes y profesoresNo hay comentarios aún
¡Sé el primero en comentar!
